Termodinâmica: primeira lei
E aconteceu que, aparecendo o sol, Deus mandou um vento calmoso oriental, e o sol feriu a cabeça de Jonas; e ele desmaiou, e desejou com toda a sua alma morrer, dizendo: Melhor me é morrer do que viver.
Jonas 4:8
Na última coluna comecei uma minissérie sobre termodinâmica. Lá comentei que o objetivo será dar base para discussão sobre cosmologia quântica: no início do universo o volume era mínimo (singular: tendendo a zero), a densidade era máxima (singular: tendendo ao infinito) e a temperatura era da ordem de 1032 K (ou graus Celsius, já que nessa escala não faz diferença). Ou seja, temos todos os problemas físicos possíveis, mas quem guiará a construção ou o surgimento dos primeiros hádrons (partículas compostas por outras, como o próton e o nêutron, que são compostos por quarks) e átomos será a termodinâmica. Inclusive, uma hipótese que pode ser colocada é que o surgimento das partículas fermiônicas (da classificação de férmions) advém através de processos termodinâmicos, como transição de fase.
Ainda na coluna anterior citei alguns processos e definições muito importantes, como processo quase-estático e calor. Ao longo desta e das outras colunas rechearei com mais definições, sempre da mesma forma: procurando ser o mais claro e sintético possível, evitando, ao máximo, equações e gráficos, que poderão ser colocados como demonstração de beleza (a física inteira é bela!) e simplificação. Com isso, já quero começar com outros conceitos muito importantes: coeficiente de dilatação, capacidade calorífica, calor específico e calor latente (ou de transformação).
Coeficiente de dilatação é uma constante e tem valor próprio para cada material ou corpo. Este coeficiente, que é um número e é incrementado a cada grau Celsius (ou por kelvin; escalas de temperatura). Exemplo: o coeficiente de expansão linear de uma barra de alumínio, a temperatura ambiente, é de 23×10-6/oC; ou seja, a cada grau Celsius a barra expande, linearmente, uma taxa de 0,0000023 a cada grau Celsius. Isso é muito importante, por exemplo, na construção de fiação pública e trilhos de trem e metrô. Observe que a fiação é maior: no frio há uma contração e no calor, uma expansão dos cabos. O mesmo vale para os trilhos e calçadas: sempre há um espaçamento de segurança.
Intuitivamente, todos os materiais, quando aquecidos, se expandem: acima acabei de falar sobre coeficiente de dilatação que cada material possui (sólidos ou líquidos, por exemplo). E esse coeficiente é para todo o espaço: linear e volumétrico. Mas, com a água a coisa é um pouco diferente: entre as temperaturas 0o e 4º graus Celsius há uma contração volumétrica, ou seja, ao invés de ter expansão, como ocorre com qualquer outro líquido, ela se contrai. E isso é facilmente observado, de forma natural, no Ártico, Antártida ou qualquer outro local que tem lagos que congelam no frio: é criado uma camada espessa de gelo na superfície e abaixo, a água está em estado líquido, tendo peixes e vida de forma abundante. Isso acontece com 2 outros satélites do nosso sistema solar: Encelado (lua de Saturno) e Europa (lua de Júpiter).
Em Europa há uma espessa camada de gelo na superfície, com rachaduras e evaporação de água (para mais detalhes, veja em https://www.nature.com/articles/s41550-019-0933-6), além dela possuir todos os ingredientes necessários para se ter vida como conhecemos (será que tem vida?).

Fonte: https://www.nasa.gov/feature/goddard/2019/nasa-scientists-confirm-water-vapor-on-europa
A outra lua que possui superfície congelada é de Júpiter: Encelado. Ela é a mais brilhante do sistema solar justamente por causa da reflexão do material congelado. E há um fenômeno muito interessante: jatos de partículas geladas quebram a superfície de gelo (média de 20 a 25 km de espessura) e sobem a uma incrível velocidade da ordem de 400 m/s (supersônica, inclusive). Esses jatos são compostos por dióxido de carbono, monóxido de carbono, água e outros ingredientes orgânicos (será que tem vida?). O interior é água líquida em uma grande quantidade: será que tem peixe?

Fonte: https://solarsystem.nasa.gov/missions/cassini/science/enceladus/
O outro conceito que mencionei acima é a capacidade calorifica: é uma outra constante (cada corpo tem um próprio) que relaciona o calor (simbolizado, em termodinâmica, pela letra Q) e a temperatura, ou seja, o objeto absorve ou elimina calor em uma dada variação de temperatura (simbolizada por ΔT). Por exemplo, a capacidade calorífica do mármore é de 749 J/K, ou seja, ele absorve / perde 749 J (joules, unidade de energia) a cada K (kelvin, temperatura). O calor específico é parecido com a capacidade calorifica, mas a massa é importante. Um exemplo: uma piscina, durante o dia e no Sol, pode ter a água mais fria; a noite, a temperatura está mais agradável, pois a água foi absorvendo energia solar durante o dia.

Fonte: https://solarsystem.nasa.gov/moons/saturn-moons/enceladus/in-depth/
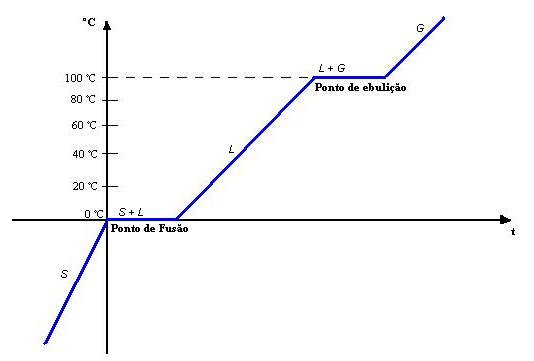
Já os calores de transformação (calor de vaporização ou calor de fusão), também conhecidos como calores latentes, estão relacionados a transição de fase: mudança de um estado para outro mantendo a sua temperatura. Por exemplo, em um copo com água e gelo, você pode ter uma temperatura de 0o grau Celsius: durante um tempo, aquecendo ou deixando o copo aberto, o gelo descongela (se transforma em água sem alterar a temperatura de 0o grau Celsius. Depois, colocando mais calor (aquecendo), a água começa a subir a temperatura. Ou seja, houve uma transição de fase (sólido para líquido) em uma temperatura constante.
Observe o gráfico abaixo. O material é água. Abaixo de 0o grau Celsius o estado físico da água é sólido (S). Durante algum tempo (t), na temperatura exata de 0o grau Celsius, temos ponto de fusão com calor de fusão e transformações do estado sólido (S) para líquido (L): não há alteração de temperatura, mas há transformação ou transição de fase. Depois da transição para líquido, a água, a partir da temperatura de 0o grau Celsius, começa a aquecer (entra em operação o calor específico) até a temperatura de 100o grau Celsius e acontece o mesmo processo: o líquido continua recebendo calor, sua temperatura não muda, mas há transição de fase para gasoso com a operação do calor latente ou de vaporização. No fim da transição, ainda em 100o grau Celsius, temos só gás de água e a temperatura pode continuar a subir, mas em um novo estado físico (gasoso).
Outro conceito que gostaria de te apresentar (ou relembrar: tudo isso pode ser visto em qualquer livro do ensino médio ou nas referências abaixo) é o trabalho. Na física, trabalho é o deslocamento de algo com aplicação de força. Por exemplo, um gás levantando ou abaixando um pistão realiza trabalho: dentro de um motor de carro, a explosão provocada por uma faísca em um reservatório com vapor de combustível empurra os pistões, realizando trabalho, para que o automóvel se movimente.

Fonte: https://www.if.ufrj.br/~bertu/fis2/segunda_lei/segunda_lei.html
Com tudo isso em mente podemos vislumbrar a Primeira Lei da Termodinâmica:
A variação de energia (ΔU) de um sistema está relacionado com a troca de calor (Q) e a realização de trabalho (W)
Permita-me apresentar apenas uma equação, que sintetiza esse enunciado, muito simples:
ΔU = ΔQ – ΔW
onde
- ΔU é a variação da energia do sistema;
- ΔQ é a variação das trocas de calor (energia) do sistema;
- ΔW é a variação do trabalho (do inglês, work) realizado / sofrido pelo sistema.
Essa primeira lei da termodinâmica está intrinsicamente relacionada com o princípio da conservação da energia ou princípio de Joule. Ou seja, no cerne da termodinâmica está o conceito de conservação. Parafraseando Lavoisier, nada no universo pode ser criado do nada: tudo é transformado e tudo é conservado. Isso tem implicações científicas e teológicas profundas. E isso é fundamental, não só na termodinâmica (lembre-se: essa área da física começou de forma experimental e nas décadas seguintes foi refinada com estudos teóricos com a mecânica estatística e a física quântica), mas em toda a física.
Há um teorema na mecânica clássica chamado teorema de Noether. Emmy Noether, a Dama da Matemática e da Física, publicou um trabalho em 1918 que é fundamental para toda a física. Em simples palavras, o teorema diz que dado um sistema mecânico (qualquer tipo de sistema que é analisado) há conservação de energia ao se fazer modificações nele. As implicações disso é que podemos rastrear como um sistema se comporta em todos os seus níveis: conhecendo a energia (tecnicamente: a lagrangiana ou a hamiltoniana) podemos saber seu comportamento e evolução.

Fonte: https://pt.wikipedia.org/wiki/Ficheiro:Noether.jpg
O universo (o que observamos), com as evidências que temos até agora, tem um tamanho finito (ordem de 46 bilhões de anos-luz de raio, considerando-o uma esfera), tem uma massa fixa e constante e uma idade finita (cerca de 13,82 bilhões de anos). Todas as medidas cosmológicas que temos até o momento, o universo é único (não há indicativo de multiverso ou outro(s) universo(s)) e tem um momento de nascimento. Mas, no séc. XX o grande cosmólogo Fred Hoyle propôs um modelo de universo onde há criação contínua de matéria com objetivo de fazê-lo eterno e imutável. Só que não há nenhuma indicação.
Talvez tenha ficado um pouco denso o texto de hoje, mas o que você precisa ter em mente é a Primeira Lei da Termodinâmica e a conservação de energia (que pode ser estendido para conservação de matéria, de números quânticos, de massa etc). Sintetizando, a Primeira Lei da Termodinâmica vai nos dizer que a variação de energia de um sistema está relacionada com a variação de calor e com a variação de trabalho. Conectando com o teorema de Noether: nada se cria do nada, tudo se transforma de algo.

Fonte: https://www.sciencenews.org/article/emmy-noether-theorem-legacy-physics-math
Mas, onde tudo isso se encaixa com a teologia? As implicações teológicas da primeira lei da termodinâmica e da lei de conservação de energia (outro nome que podemos usar para o teorema de Noether), com aplicação cosmológica está relacionado com a criação de toda a natureza: “no princípio Deus criou todas as coisas”, é assim que começa o texto bíblico. A Doutrina Cristã da Criação, onde McGrath desenvolve no livro A ciência de Deus: uma introdução à Teologia Científica, parte do pressuposto bíblico e se conecta com o que conhecemos na cosmologia observacional. Ou seja, tudo foi criado por Deus e nada do que existe está fora de Suas mãos. Contudo, Ele utilizou métodos físicos muito bem definidos; nós, físicos cristãos, acreditamos que estamos descobrindo alguns desses processos.
E Deus os abençoou, dizendo: Frutificai e multiplicai-vos, e enchei as águas nos mares; e as aves se multipliquem na terra.
Gênesis 1:22
Só isso?! Sim! Mas, ficou em dúvida, quer perguntar algo, deixar algum comentário ou sugerir algum tema, deixe abaixo! Ficarei feliz em te responder, seja nos comentários ou em algum artigo específico.
Sugestão de leitura
Para essa minissérie estou utilizando os livros abaixo. O nível deles é de início de graduação à pós, inclusive estudei em dois deles no doutorado:
- Termodinâmica, por Mário José de Oliveira, 2ª edição revista e ampliada, editora Livraria da Física;
- Foundations of statistical mechanics: a deductive treatment, por Oliver Penrose, editora Pergamon Press. Oliver Penrose é irmão do físico Roger Penrose, que ganhou o Nobel de Física este ano, 2020, pelo desenvolvimento matemático com a RG sobre os buracos negros;
- Introducton to statistical physics, por Kerson Huang, editora Taylor & Francis;
- Introdução à física estatística, por Sílvio Salinas, editor EdUSP. Prof. Salinas é uma referência em física estatística no Brasil;
- Fundamentos de física: gravitação, ondas e termodinâmica, por Halliday, Resnick e Walker, vol. 2, 7ª edição, editora LTC. É o tradicional livro (ou coleção: são 4 volumes no total) introdutório a física para quem quer algo a mais do que aprendeu no ensino médico ou está entrando na faculdade;
- Curso de física estatística, por Torsten Fließbach (ß tem um som ou pode ser transliterado por ss: Fliessbach), editora Fundação Calouste Gulbenkian.
As recomendações de leitura, que não são acadêmicas:
- Livro A ciência de Deus: uma introdução à Teologia Científica, por Alister McGrath, editora Ultimato em parceria com a Associação Brasileira de Cristãos na Ciência;
- Um bom texto para complementar esse tema com relação à motivação de Hoyle pode ser visto aqui https://www.cristaosnaciencia.org.br/a-teoria-do-big-bang-e-os-100-anos-da-relatividade-geral/;
- Livro Astronomia e astrofísica, por S. O. Kepler e Maria de Fátima Saraiva. Este livro é disponibilizado no próprio site dos autores, que são professores da UFRGS. É um excelente material de consulta: http://astro.if.ufrgs.br/livro.pdf;
- Livro Alfa e Ômega: a busca pelo início e fim do universo, por Charles Seife, editora Roccomn. É um livro de 2007, está um pouquinho desatualizado com relação a dados (como bóson de Higgs e ondas gravitacionais), mas ainda é muito proveitoso e com uma didática muito boa;
- Livro Cosmologia física: do micro ao macro cosmos e vice-versa, por Jorge Horvath, German Lugones, Marcelo porto, Sergio Scarano e Ramachrisna Teixeira, editora Livraria da Física. Outro livro muito bom, um pouquinho técnico, mas nada que não possa ser resolvido por si mesmo. Está um pouquinho desatualizado com relação a dados por ser de 2011, porém, altamente recomendado;
- Prof. Alexandre Zabot, da UFSC, tem um curso gratuito de astrofísica geral excelente. Recomendo fortemente. Você assiste as aulas no YouTube, tem acesso ao material (slides, sites e alguns textos). Para todas as informações, links das aulas e materiais: https://astrofisica.ufsc.br/astrofisica-geral/.